Органическая химия, стр. 11
Органическая химия (Грандберг И. И.)
06.10.2007
В учебнике большое внимание уделяется общетеоретическим основам современной органической химии: строению органических соединений, механизмам реакций, современным физико-химическим и физическим методам исследования. Для книги характерны ярко выраженная биологическая направленность и высокий научный уровень. Четвертое издание переработано и расширено. Это коснулось механизмов реакций, физико-химических методов исследования, химии гетероциклов, оптической изомерии раздела о ферментах, физиологически активных соединений. Учебник дополнен приложением «Основы принципа сохранения симметрии молекулярных орбиталей». Книга предназначена для студентов вузов, обучающихся по агрономическим специальностям. Может быть использована студентами других сельскохозяйственных, а также биологических специальност...
15.51М, RUS.
В учебнике большое внимание уделяется общетеоретическим основам современной органической химии: строению органических соединений, механизмам реакций, современным физико-химическим и физическим методам исследования. Для книги характерны ярко выраженная биологическая направленность и высокий научный уровень. Четвертое издание переработано и расширено. Это коснулось механизмов реакций, физико-химических методов исследования, химии гетероциклов, оптической изомерии раздела о ферментах, физиологически активных соединений. Учебник дополнен приложением «Основы принципа сохранения симметрии молекулярных орбиталей». Книга предназначена для студентов вузов, обучающихся по агрономическим специальностям. Может быть использована студентами других сельскохозяйственных, а также биологических специальност...
15.51М, RUS.
Cyclic Voltammetry: Simulation and Analysis of Reaction Mechanisms (Gosser D. K., Jr.)
06.10.2007
Cyclic voltammetry (CV) has been in the forefront of the study of electron transfer and its consequences. With the cyclic voltammetric method one can simultaneously activate molecules by electron transfer and probe subsequent chemical reactions. The cyclic voltammetric response curve thus provides information about electron transfer kinetics and thermodynamics as well as the consequences of electron transfer. This book introduces cyclic voltammetry and its application to the analysis of electrochemical reaction mechanisms. It also provides the experimentalist with a simulation-based approach for the analysis of cyclic voltammograms.
8.2М, ENG.
Cyclic voltammetry (CV) has been in the forefront of the study of electron transfer and its consequences. With the cyclic voltammetric method one can simultaneously activate molecules by electron transfer and probe subsequent chemical reactions. The cyclic voltammetric response curve thus provides information about electron transfer kinetics and thermodynamics as well as the consequences of electron transfer. This book introduces cyclic voltammetry and its application to the analysis of electrochemical reaction mechanisms. It also provides the experimentalist with a simulation-based approach for the analysis of cyclic voltammograms.
8.2М, ENG.
Некоторые принципы синтеза гетероциклических соединений (Голубчиков О. А.)
06.10.2007
Изложены основные принципы синтеза гетероциклических соединений. Описывается механизм ключевых стадий построения гетероциклов. Особое внимание уделено синтезам пиридинового, хинолинового, пиррольного и порфиринового гетероциклов. Кратко рассмотрены методы очистки соединений.
0.49М, RUS.
Изложены основные принципы синтеза гетероциклических соединений. Описывается механизм ключевых стадий построения гетероциклов. Особое внимание уделено синтезам пиридинового, хинолинового, пиррольного и порфиринового гетероциклов. Кратко рассмотрены методы очистки соединений.
0.49М, RUS.
Практикуп по органическомк синтезу (Голодовников Г. В., Мандельштам Т. В.)
06.10.2007
Учебное пособие составлено на основе опыта проведения практикума по органическому синтезу на химическом факультете Ленинградского университета. Дано описание синтезов более 160 препаратов, причем 30 методик излагаются в практикуме впервые. Приводятся основные методы выделения, очистки и идентификации органических веществ. В отличие от существующих отечественных пособий в книге методы синтеза препаратов сгруппированы по признаку общности механизма реакции, что позволяет лучше систематизировать фактический материал органической химии и теснее связать теорию с практикой органического синтеза. Описанию практических работ в каждой главе предшествует общая часть, знакомящая с современными представлениями о механизме рассматриваемых реакций и дающая характеристику основных синтетических методов. ...
2.42М, RUS.
Учебное пособие составлено на основе опыта проведения практикума по органическому синтезу на химическом факультете Ленинградского университета. Дано описание синтезов более 160 препаратов, причем 30 методик излагаются в практикуме впервые. Приводятся основные методы выделения, очистки и идентификации органических веществ. В отличие от существующих отечественных пособий в книге методы синтеза препаратов сгруппированы по признаку общности механизма реакции, что позволяет лучше систематизировать фактический материал органической химии и теснее связать теорию с практикой органического синтеза. Описанию практических работ в каждой главе предшествует общая часть, знакомящая с современными представлениями о механизме рассматриваемых реакций и дающая характеристику основных синтетических методов. ...
2.42М, RUS.
Синтез пептидов. Реагенты и методы (Гершкович А. А., Кибирев В. К.)
06.10.2007
Монография посвящена современным методам и реагентам, используемым для синтеза пептидов. Приводятся техника и методика получения конденсирующих средств, отражены способы защиты и деблокирования функциональных групп аминокислот и пептидов. Оскществлена классификация реагентов по принципу химического строения. Кратко описываются механизмы активации карбоксильной группы, реакций образования пептидных связей и процессов, происходящих при удалении защитных групп.
6.55М, RUS.
Монография посвящена современным методам и реагентам, используемым для синтеза пептидов. Приводятся техника и методика получения конденсирующих средств, отражены способы защиты и деблокирования функциональных групп аминокислот и пептидов. Оскществлена классификация реагентов по принципу химического строения. Кратко описываются механизмы активации карбоксильной группы, реакций образования пептидных связей и процессов, происходящих при удалении защитных групп.
6.55М, RUS.
Синтезы гетероциклических соединений. Выпуск 12 (Мнджоян А. Л.)
06.10.2007
Настоящий сборник является двенадцатым выпуском периодической серии «Синтезы гетероциклических соединений», который по примеру предыдущих выпусков содержит описание тридцати методов получения различных гетероциклов с гетероатомами азотом, кислородом, серой. Тщательно проверенные методы получения производных фурана, имидазола, тиазола, пиридина, пиримидина, индола, изохинолина, пирана и др. предложены в основном сотрудниками Института тонкой органической химии им. А. Л. Мнджояна АН Армянской ССР, а также коллегами из других городов нашей страны. Предлагаемые методики представляют интерес для широкого круга химиков-органиков, занятых как исследовательской работой, так и производством химических реактивов.
0.51М, RUS.
Настоящий сборник является двенадцатым выпуском периодической серии «Синтезы гетероциклических соединений», который по примеру предыдущих выпусков содержит описание тридцати методов получения различных гетероциклов с гетероатомами азотом, кислородом, серой. Тщательно проверенные методы получения производных фурана, имидазола, тиазола, пиридина, пиримидина, индола, изохинолина, пирана и др. предложены в основном сотрудниками Института тонкой органической химии им. А. Л. Мнджояна АН Армянской ССР, а также коллегами из других городов нашей страны. Предлагаемые методики представляют интерес для широкого круга химиков-органиков, занятых как исследовательской работой, так и производством химических реактивов.
0.51М, RUS.
Синтезы гетероциклических соединений. Выпуск 11 (Мнджоян А. Л.)
06.10.2007
Одиннадцатый выпуск серии «Синтезы гетероциклических соединений» содержит описание тридцати тщательно проверенных методов получения различных производных пиррола, фурана, тетрагидрофурана, пиперидина, тетрагидропирана, имидазола, пиримидина, а также конденсированных гетероциклических систем. В разработке материалов сборника участвовали сотрудники Института тонкой органической химии им. А. Л.Мнджояна АН Армянской ССР и ряд ученых Советского Союза и зарубежных стран. Приведенные методы представляют интерес как для исследовательских работ, так и для производства химических реактивов. При составлении раздела «Другие способы получения» использована литература до 1974 г. включительно.
0.53М, RUS.
Одиннадцатый выпуск серии «Синтезы гетероциклических соединений» содержит описание тридцати тщательно проверенных методов получения различных производных пиррола, фурана, тетрагидрофурана, пиперидина, тетрагидропирана, имидазола, пиримидина, а также конденсированных гетероциклических систем. В разработке материалов сборника участвовали сотрудники Института тонкой органической химии им. А. Л.Мнджояна АН Армянской ССР и ряд ученых Советского Союза и зарубежных стран. Приведенные методы представляют интерес как для исследовательских работ, так и для производства химических реактивов. При составлении раздела «Другие способы получения» использована литература до 1974 г. включительно.
0.53М, RUS.
Синтезы гетероциклических соединений. Выпуск 10 (Мнджоян А. Л.)
06.10.2007
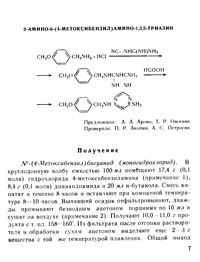
N1-(4-Метоксибензил)бигуанид (моногидрохлорид). В круглодонную колбу емкостью 100 мл помещают 17,4 г (0,1 моля) гидрохлорида 4-метоксибензиламнна, 8,4 г (0,1 моля) дициандиамида и 20 мл н-бутанола. Смесь кипятят в течение 8 часов и оставляют при комнатной температуре 8—10 часов. Выпавший осадок отфильтровывают, дважды промывают безводным ацетоном порциями по 10 мл и сушат на воздухе. Получают 10,0 — 11,0 г продукта с т. пл. 158—160°. Из фильтрата после отгонки растворителя и обработки сухим ацетоном выделяют еще 2-3 г вещества с той же температурой плавления. Общий выход составляет 12,0—13,0 г, или 46,5—50,4% теоретического количества. Тяжелые будни химиков. Часть 10.
0.51М, RUS.
N1-(4-Метоксибензил)бигуанид (моногидрохлорид). В круглодонную колбу емкостью 100 мл помещают 17,4 г (0,1 моля) гидрохлорида 4-метоксибензиламнна, 8,4 г (0,1 моля) дициандиамида и 20 мл н-бутанола. Смесь кипятят в течение 8 часов и оставляют при комнатной температуре 8—10 часов. Выпавший осадок отфильтровывают, дважды промывают безводным ацетоном порциями по 10 мл и сушат на воздухе. Получают 10,0 — 11,0 г продукта с т. пл. 158—160°. Из фильтрата после отгонки растворителя и обработки сухим ацетоном выделяют еще 2-3 г вещества с той же температурой плавления. Общий выход составляет 12,0—13,0 г, или 46,5—50,4% теоретического количества. Тяжелые будни химиков. Часть 10.
0.51М, RUS.
Синтезы гетероциклических соединений. Выпуск 9 (Мнджоян А. Л.)
06.10.2007
Девятый выпуск серии «Синтезы гетероциклических соединений» содержит описание методов получения тридцати различных производных пиразола, пиримидина, хинолина, изохииолина, тиазола, имидазола и других гетероциклических систем. При подборе методов для комплектования девятого выпуска редколлегия, как и прежде, руководствовалась такими признаками, как оригинальность проведения синтеза, доступность исходных веществ и возможность широкого применения получаемых соединений в органическом синтезе. Часть описываемых методов разработана и предложена сотрудниками Института тонкой органической химии АН Армянской ССР и другими советскими и зарубежными учеными. При подготовке остальной части прописей использованы материалы, опубликованные в литературе, но при этом проводилась тщательная проверка методов ...
0.52М, RUS.
Девятый выпуск серии «Синтезы гетероциклических соединений» содержит описание методов получения тридцати различных производных пиразола, пиримидина, хинолина, изохииолина, тиазола, имидазола и других гетероциклических систем. При подборе методов для комплектования девятого выпуска редколлегия, как и прежде, руководствовалась такими признаками, как оригинальность проведения синтеза, доступность исходных веществ и возможность широкого применения получаемых соединений в органическом синтезе. Часть описываемых методов разработана и предложена сотрудниками Института тонкой органической химии АН Армянской ССР и другими советскими и зарубежными учеными. При подготовке остальной части прописей использованы материалы, опубликованные в литературе, но при этом проводилась тщательная проверка методов ...
0.52М, RUS.
Синтезы гетероциклических соединений. Выпуск 8 (Мнджоян А. Л.)
06.10.2007
Восьмой выпуск серии «Синтезы гетероциклических соединений» содержит описание методов получения различных типов гетероциклических соединений—фурана, индола, пирилина, пиримидина, тиазола, хинолина, имидазола и др. По примеру предыдущих выпусков настоящий, восьмой, выпуск включает в себя тридцать методов, предложенных сотрудниками Института тонкой органической химии, а также другими авторами—советскими и зарубежными. Приведенные методы представляют интерес как для исследовательских работ, так и для промышленности химических реактивов. При составлении раздела «Другие способы получения» использована литература до 1966 г. включительно.
0.82М, RUS.
Восьмой выпуск серии «Синтезы гетероциклических соединений» содержит описание методов получения различных типов гетероциклических соединений—фурана, индола, пирилина, пиримидина, тиазола, хинолина, имидазола и др. По примеру предыдущих выпусков настоящий, восьмой, выпуск включает в себя тридцать методов, предложенных сотрудниками Института тонкой органической химии, а также другими авторами—советскими и зарубежными. Приведенные методы представляют интерес как для исследовательских работ, так и для промышленности химических реактивов. При составлении раздела «Другие способы получения» использована литература до 1966 г. включительно.
0.82М, RUS.
Синтезы гетероциклических соединений. Выпуск 7 (Мнджоян А. Л.)
06.10.2007
Седьмой выпуск серии «Синтезы гетероциклических соединений», помимо ранее использованных гетероциклических систем: тиазола, индола, пиридина, хинолина и других, содержит методы синтеза производных тиофена, пиримидина, бензодиоксана, бензотиазола, оксадиазола и других гетероциклических систем. Эти соединения сегодня представляют интерес для получения физиологически активных препаратов, красителей и полимерных веществ. По примеру предыдущих выпусков седьмой выпуск сборника содержит тридцать методов, из которых часть предложена сотрудниками Института тонкой органической химии и другими авторами, остальная часть отобрана из литературных источников и включена в сборник после проверки и внесения нужных коррективов, обеспечивающих хорошие выходы и воспроизводимость метода.
0.74М, RUS.
Седьмой выпуск серии «Синтезы гетероциклических соединений», помимо ранее использованных гетероциклических систем: тиазола, индола, пиридина, хинолина и других, содержит методы синтеза производных тиофена, пиримидина, бензодиоксана, бензотиазола, оксадиазола и других гетероциклических систем. Эти соединения сегодня представляют интерес для получения физиологически активных препаратов, красителей и полимерных веществ. По примеру предыдущих выпусков седьмой выпуск сборника содержит тридцать методов, из которых часть предложена сотрудниками Института тонкой органической химии и другими авторами, остальная часть отобрана из литературных источников и включена в сборник после проверки и внесения нужных коррективов, обеспечивающих хорошие выходы и воспроизводимость метода.
0.74М, RUS.
Синтезы гетероциклических соединений. Выпуск 6 (Мнджоян А. Л.)
06.10.2007
Шестой выпуск серии „Синтезы гетероциклических соединений" содержит разработанные или проверенные в Институте тонкой органической химии Академии наук Армянской ССР методы получения производных кислород-, серу- и азотсодержащих гетероциклических систем, в частности фурана, диоксана, тиазола, пиридина, хинолина, индола, имидазола, триазола и др. Соединения, описанные в шестом выпуске, как и материалы предыдущих сборников, могут представить интерес для химиков-органиков в качестве промежуточных веществ в синтетических работах. При составлении разделов „Другие способы получения" использовалась литература до 1961 г. включительно.
0.67М, RUS.
Шестой выпуск серии „Синтезы гетероциклических соединений" содержит разработанные или проверенные в Институте тонкой органической химии Академии наук Армянской ССР методы получения производных кислород-, серу- и азотсодержащих гетероциклических систем, в частности фурана, диоксана, тиазола, пиридина, хинолина, индола, имидазола, триазола и др. Соединения, описанные в шестом выпуске, как и материалы предыдущих сборников, могут представить интерес для химиков-органиков в качестве промежуточных веществ в синтетических работах. При составлении разделов „Другие способы получения" использовалась литература до 1961 г. включительно.
0.67М, RUS.
Синтезы гетероциклических соединений. Выпуск 5 (Мнджоян А. Л.)
06.10.2007
В пятом выпуске серии «Синтезы гетероциклических соединений» описываются проверенные методы получения тридцати производных фурана, бензофурана, пиридина, хинолина, тиазола и др. При подборе материалов для настоящего сборника редколлегия стремилась выбрать те производные гетероциклов, которые по своему строению могут представить интерес в качестве промежуточных веществ в органическом синтезе. Часть описываемых методов разработана и предложена сотрудниками Института тонкой органической химии. Для разработки другой части методов использованы литературные материалы, но при этом проводилась тщательная проверка, а подчас вносились изменения в описанные синтезы.
0.87М, RUS.
В пятом выпуске серии «Синтезы гетероциклических соединений» описываются проверенные методы получения тридцати производных фурана, бензофурана, пиридина, хинолина, тиазола и др. При подборе материалов для настоящего сборника редколлегия стремилась выбрать те производные гетероциклов, которые по своему строению могут представить интерес в качестве промежуточных веществ в органическом синтезе. Часть описываемых методов разработана и предложена сотрудниками Института тонкой органической химии. Для разработки другой части методов использованы литературные материалы, но при этом проводилась тщательная проверка, а подчас вносились изменения в описанные синтезы.
0.87М, RUS.
Синтезы гетероциклических соединений. Выпуск 4 (Мнджоян А. Л.)
06.10.2007
В литровый стакан, снабженный мешалкой и погруженный в баню со смесью льда и соли, помещают раствор 37,5 г (0,935 моля) едкого натра в 400 мл воды. К этому раствору прибавляют при перемешивании 47,9 г (15,1 мл, 0,3 моля) брома. Когда температура смеси достигает 0C, к ней прибавляют в один прием, при сильном перемешивании, 30,0 г (0,245 моля) никотинамида (примечание 1). После 15-минутного перемешивания раствор становится прозрачным. Тяжелые будни армянских химиков. Выпуск 4.
1.01М, RUS.
В литровый стакан, снабженный мешалкой и погруженный в баню со смесью льда и соли, помещают раствор 37,5 г (0,935 моля) едкого натра в 400 мл воды. К этому раствору прибавляют при перемешивании 47,9 г (15,1 мл, 0,3 моля) брома. Когда температура смеси достигает 0C, к ней прибавляют в один прием, при сильном перемешивании, 30,0 г (0,245 моля) никотинамида (примечание 1). После 15-минутного перемешивания раствор становится прозрачным. Тяжелые будни армянских химиков. Выпуск 4.
1.01М, RUS.
Синтезы гетероциклических соединений. Выпуск 3 (Мнджоян А. Л.)
06.10.2007
Хлористоводородная 8-(5-карбэтоксифурфурил)тиомочевина. В круглодонную колбу емкостью 250 мл, снабженную обратным холодильником с хлоркальциевой трубкой, помещают 37,7 г (0,2 моля) свежеперегнанного этилового эфира 5-хлорметилфуран-2-карбоноврй кислоты, 15,2 г (0,2 моля) тиомочевины и 40 мл абсолютного метилового спирта. Смесь кипятят на водяной бане в течение 4—5 часов, после чего в горячем состоянии сливают в полулитровый стакан и колбу споласкивают 5 мл абсолютного метилового спирта, которые присоединяют к основному продукту. При охлаждении проточной водой и помешивании стеклянной палочкой приливают 175—200 мл абсолютного эфира. Армянская алхимия. Выпуск 3.
0.75М, RUS.
Хлористоводородная 8-(5-карбэтоксифурфурил)тиомочевина. В круглодонную колбу емкостью 250 мл, снабженную обратным холодильником с хлоркальциевой трубкой, помещают 37,7 г (0,2 моля) свежеперегнанного этилового эфира 5-хлорметилфуран-2-карбоноврй кислоты, 15,2 г (0,2 моля) тиомочевины и 40 мл абсолютного метилового спирта. Смесь кипятят на водяной бане в течение 4—5 часов, после чего в горячем состоянии сливают в полулитровый стакан и колбу споласкивают 5 мл абсолютного метилового спирта, которые присоединяют к основному продукту. При охлаждении проточной водой и помешивании стеклянной палочкой приливают 175—200 мл абсолютного эфира. Армянская алхимия. Выпуск 3.
0.75М, RUS.